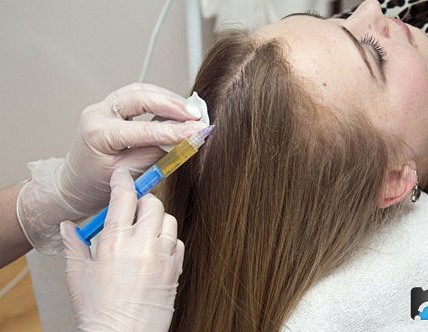
Регенеративная медицина — современное динамичное направление в терапии различных патологий, формирующееся на стыке биологии, биоинженерии и практической медицины.
Методы регенеративной медицины направлены на стимуляцию процессов восстановления утраченной функции — либо через мобилизацию стволовых клеток самого организма, либо путем введения аллогенного (донорского) клеточного материала. В последнее время большое распространение получил метод плазмотерапии.
Плазмотерапией называют использование в лечебных или косметических целях плазмы, полученной из аутологичной крови человека. Получение материала (плазмы) из собственной крови пациента обеспечивает безопасность лечения, так как в этом случае отсутствует опасность инфицирования и мутагенного эффекта.
Существует несколько методик плазмотерапии:
- — плазмолифтинг (англ. «рlasmolifting»)
- — применение активированной (или неактивированной) — аутологичной плазмы крови, обогащенной тромбоцитарными факторами роста (АОТ, Platelet-Rich-Plasma — PRP)
Лечебные эффекты плазмотерапии основываются на высвобождении из тромбоцитов — плоских безъядерных клеток, циркулирующих в кровотоке со сроком жизни 7–10 дней, в концентрации 150–400 тыс/мкл — различных факторов роста (ФР)— гормоноподобных полипептидов с широким спектром биологического действия, способных стимулировать или ингибировать митоз, хемотаксис, дифферен цировку клеток.
В цитоплазме тромбоцитов содержатся такие структуры, как электронно-плотные тельца, лизосомы и альфа-гранулы, в которых депонируется большое количество факторов роста, цитокинов, хемокинов и адгезивных белков (фибриноген, фибрин и др.). Основные факторы роста содержатся в альфа-гранулах и высвобождаются посредством экзоцитоза после активации тромбоцита и действуют локально, не существуя в свободной форме в кровотоке, те есть в обычных или стандартных условиях работы организма.
Понятие «плазмотерапии» и ее лечебные эффекты.
Плазмотерапией называют использование в лечебных или косметических целях плазмы, полученной из аутологичной крови человека. Получение материала (плазмы) из собственной крови пациента обеспечивает безопасность лечения, так как в этом случае отсутствует опасность инфицирования и мутогенного эффекта.
Существует несколько методик плазмотерапии:
- плазмолифтинг (англ. «рlasmolifting»);
- применение активированной (или неактивированной) — аутологичной плазмы крови, обогащенной тромбоцитарными факторами роста (АОТ, Platelet—Rich—Plasma — PRP).
Лечебные эффекты плазмотерапии основываются на высвобождении из тромбоцитов — плоских безъядерных клеток, циркулирующих в кровотоке со сроком жизни 7–10 дней, в концентрации 150–400 тыс/мкл — различных ФР — гормоноподобных полипептидов с широким спектром биологического действия, способных стимулировать или ингибировать митоз, хемотаксис, дифференцировку клеток. В цитоплазме тромбоцитов содержатся такие структуры, как электронно-плотные тельца, лизосомы и альфа-гранулы, в которых депонируется большое количество ФР, цитокинов, хемокинов и адгезивных белков (фибриноген, фибрин и др.).
Основные ФР содержатся в альфа-гранулах и высвобождаются посредством экзоцитоза после активации тромбоцита и действуют локально, не существуя в свободной форме в кровотоке. К настоящему времени известно более 30 ФР. Эффекты самых важных из них описаны в таблице.
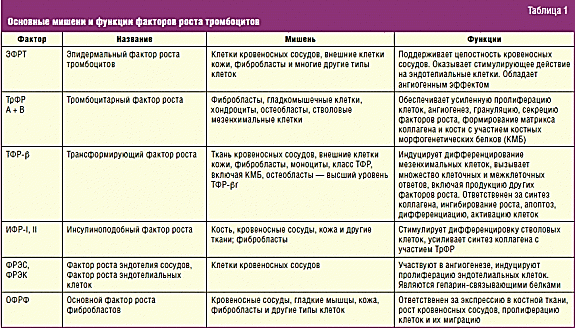
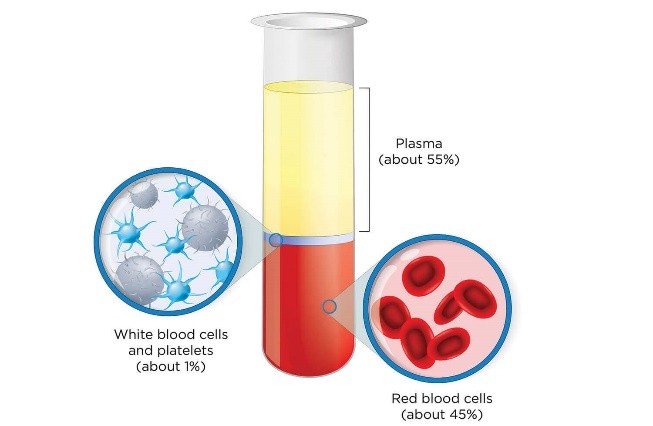
Основными физиологическими активаторами тромбоцитов являются: коллаген (главный белок внеклеточного матрикса), тромбин (сериновая протеиназа, центральный фермент плазменной системы свертывания), АДФ (адениновый нуклеотид, который выделяется из разрушенных клеток сосуда или секретируется плотными гранулами самих тромбоцитов), а также тромбоксан А2 — липид из класса эйкозаноидов, синтезируемый и выделяемый тромбоцитами. Действие каждого из тромбоцитарных активаторов опосредуется через специализированные рецепторы в мембране тромбоцита. В последние годы было установлено, что Са2+ также играет важную роль в активации тромбоцитов, поэтому для оптимизации высвобождения ФР наиболее часто используют хлорид (иногда глюконат) кальция или собственный тромбин. Активация также может происходить за счет механического или температурного воздействия.
Активация плазмы приводит к высвобождению тромбоцитами ФР, а также к полимеризации фибрина, после чего из суспензии PRP образуется гель. Высвобождаемые ФР (естественные полипептиды) воздействуют на клетки-мишени с высокой аффинностью, создавая оптимальную среду для регенерации и репарации тканей. Известно, что лечебный эффект достигается при концентрации тромбоцитов в плазме от 750 тыс. до 1 млн клеток на 1 мкл плазмы.
Плазмолифтинг
При плазмолифтинге используется способ отделения цельной плазмы, аналогичный таковому при выполнении стандартных лабораторных исследований. Применяются обычные центрифуги и пробирки. Поэтому при приготовлении аутоплазмы клеточные оболочки клеток крови разрушаются, и в результате получается плазма, взвесь клеточных фрагментов и небольшое количество сохранившихся клеток. Лечебный эффект плазмолифтинга зависит от количества сохранных тромбоцитов. Считается, что высокая концентрация тромбоцитов в очаге введения достигается путем увеличения объема инъекционно вводимой плазмы, поэтому в очаге инъекций концентрация тромбоцитов больше, чем в циркулирующей крови. Также технология плазмолифтинга не предусматривает активацию тромбоцитов.
Аутологичная плазма крови, обогащенная тромбоцитарными факторами роста (PRP)
Методика PRP патогенетически обоснована больше чем плазмолифтин, так как именно повышенная концентрация тромбоцитов, а не количество введенной плазмы запускает регенеративные способности организма. При PRP-терапии аутоплазма обогащается тромбоцитами за счет применения технологий «мягкого» центрифугирования в специальных пробирках в форме песочных часов.
.
В зависимости от биохимической структуры, получаемой с помощью различных методик и оборудования, PRP-препараты могут быть нескольких видов:
- PRP (Platelet Rich Plasma) — суспензия;
- PRG (Platelet Rich Gel) — обогащенный тромбоцитами гель (активированная суспензия, в которой фибриноген преобразуется в фибрин в виде слабо сшитых волокон);
- PRF (Platelet Rich Fibrin) — обогащенный тромбоцитами фибрин плазмы крови в виде сшитой фибриновой сети высокой плотности;
- PRFM (Platelet Rich Fibrin Matrix) — представляет собой трехмерный фибриновый матрикс с высокой плотностью и степенью полимеризации фибрина за счет обогащения плазмы не только тромбоцитами, но и фибриногеном, с последующей активацией тромбоцитов. При этом сепарация клеточных компонентов происходит без использования антикоагулянтов.
Области применения плазмотерапии
Плазмотерапия с успехом применяется в различных областях медицины. В травматологии PRP применяется при лечении артрозов, артритов, эпикондилитов, субакромиального синдрома, плантарного фасциита («пяточных шпор»); при этом реализуется спазмолитический эффект, восстанавливаются объем и состав суставной жидкости, активируется кровообращение в области пораженного сустава, укрепляются связки и мышцы, окружающие больной сустав.
G. Bosh и соавт. в эксперименте с травмами сухожилий у лошадей исследовали влияние PRP на неоваскуляризацию и показали, что PRP способствует ангиогенезу.
Доказана эффективность PRP-терапии в составе комплексного лечения хронических заболеваний органов малого таза, аднекситов, эндометритов в гинекологии. С помощью препаратов аутоплазмы, обогащенной факторами роста удалось решить проблемы так называемого «тонкого эндометрия» и эндометрия с низким имплантационным потенциалом. Благодаря этому удалось значительно увеличить результативность программ лечения бесплодия методом ЭКО.
Наиболее новым направлением применением PRP-препаратов в репродуктологии – лечение преждевременного истощения яичников различного генеза. Это единственный обнадеживающий клинический подход, который имеет доказанные положительные результаты восстановления работы яичников при снижении уровня гормона АМГ ниже 0,2 нг\мл.
В стоматологии метод PRP-терапии успешно применяется для лечения воспалительных заболеваний — гингивитов, парадонтитов и др., а также при операциях удаления зубов и имплантациях. Уже через несколько процедур можно увидеть положительную динамику от лечения в виде улучшения показателей гигиенических и пародонтологических индексов, снижения кровоточивости десен.
Благодаря противовоспалительному, анальгетическому, противоотечному и гемостатическому эффектам PRP, сопоставимым с эффектом кортикостероидной терапии, данный метод нашел широкое применение в хирургии. Способность запускать ангиогенез открывает новые возможности в кардиохирургии при введении PRP в очаги ишемизации у пациентов с инфарктом миокарда.

В офтальмологии PRP используют при лечении язв роговицы — показано, что аутоплазма, обогащенная тромбоцитами, способствует уменьшению воспаления, боли и субъективных ощущений.
Но, пожалуй, активнее всего аутологичная плазма крови, обогащенная тромбоцитарными факторами роста, используется в пластической хирургии, дерматологии и косметологии,
так как очевидно, что факторы роста, цитокины и другие биологически активные вещества способны оказывать нормализующее влияние на процессы репарации и регенерации тканей.
Поскольку факторы роста могут воздействовать на стволовые клетки в области фолликула волоса, стимулируя развитие новых фолликулов, способствуют неоваскуляризации и пролонгируют фазу анагеновой фазы роста волоса (период интенсивного деления клеток волосяного фолликула), PRP активно используется в трихологии (лечение выпадения волос различного происхождения).